Niet alle virussen maken ons ziek
Na de lockdown is het bijna niet te geloven dat er ook virussen zijn die ons leven kunnen redden. Toch bestaan ze.
Stan Brouns van de TU Delft onderzoekt bacteriofagen, virussen die bacteriën onschadelijk maken. Alles staat gereed voor medisch onderzoek naar fagen als behandeling van bacteriële infecties, alleen vormen Nederlandse regels nog een groot obstakel.
Eerlijk gezegd had Stan Brouns, universitair docent moleculaire microbiologie aan de TU Delft, twaalf jaar geleden geen idee van de mogelijkheden van bacteriofagen voor de gezondheidszorg. Hij startte toen in Wageningen met fundamenteel onderzoek naar een verdedigingsmechanisme van bacteriën tegen vijandelijke virussen zoals bacteriofagen.
Na verloop van tijd begon hij te begrijpen dat bacteriofagen een oplossing kunnen bieden voor antibioticaresistentie. Bacteriën die resistent zijn geworden tegen een heel scala aan antibiotica zijn namelijk vaak nog wel aan te pakken met fagen.
Het grote publiek heeft door de televisieprogramma’s Zorg Nu en Dokters van Morgen van Antoinette Hertsenberg een groeiende belangstelling voor bacteriofagen. In deze programma’s worden mensen gevolgd die last hebben van hardnekkige bacteriële infecties. Sommigen stonden al met één been in graf en genazen dankzij bacteriofagen.
Maanlandertjes
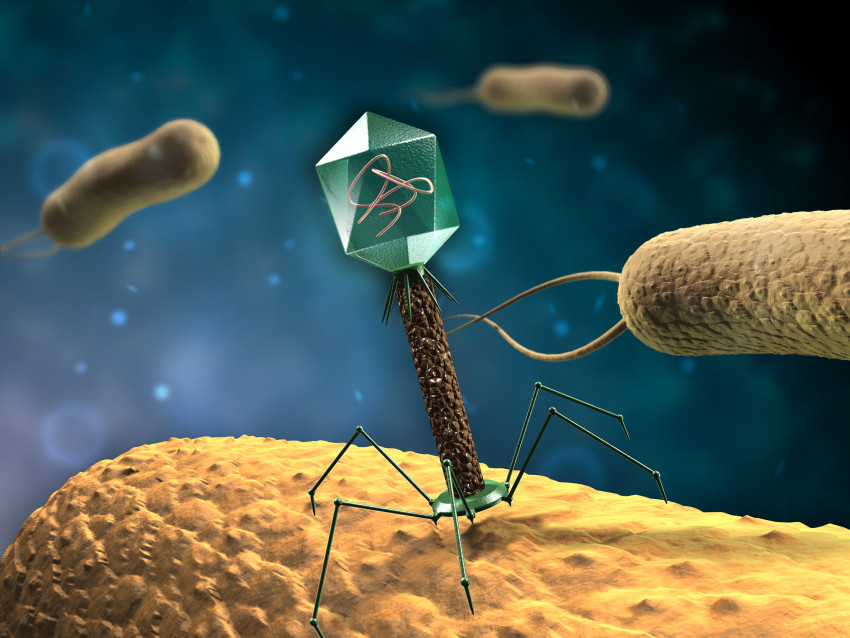
Wat zijn bacteriofagen nu precies? Net als het coronavirus is een bacteriofaag een virus, maar dan eentje die exclusief voor bacteriën kiest als slachtoffer. Bacteriofagen zien er ook totaal anders uit dan coronavirussen: het zijn geen bolletjes met zuignappen maar meer een soort maanlandertjes. Ze hebben een hoekige kop gevuld met DNA (of RNA), een lange nek en spinachtige poten. Met deze poten landt een bacteriofaag op een bacterie om zijn genetische materiaal te injecteren.
Razendsnel vermenigvuldigt de faag zich in de gastheer, gebruikmakend van de machinerie in de bacteriecel. Vervolgens wordt er een enzym aangemaakt dat zorgt dat de bacterie openbreekt en de nakomelingen van de faag op zoek kunnen gaan naar nieuwe slachtoffers. Fagen zijn specialisten: ieder type faag richt zich uitsluitend op één type bacterie.
Oostblok
Fagen inzetten om infecties bij mensen te bestrijden is niet nieuw. De Frans-Canadese microbioloog Félix d’Hérelle ontdekte al rond 1920 dat fagen korte metten konden maken met bacteriële infecties en ontwikkelde een succesvolle faagtherapie. Antibiotica streefden de faagtherapie al snel voorbij omdat ze meerdere bacteriën tegelijk kunnen bestrijden. Bij faagtherapie moet je eerst bepalen welk type bacterie voor de problemen zorgt en daar vervolgens een bijpassende faag bij vinden.
Alleen in het toenmalige Oostblok is na de Tweede Wereldoorlog de toepassing van faagtherapie en het onderzoek naar bacteriofagen voortgezet. Deze landen konden moeilijk aan antibiotica komen en de fagen boden uitkomst.
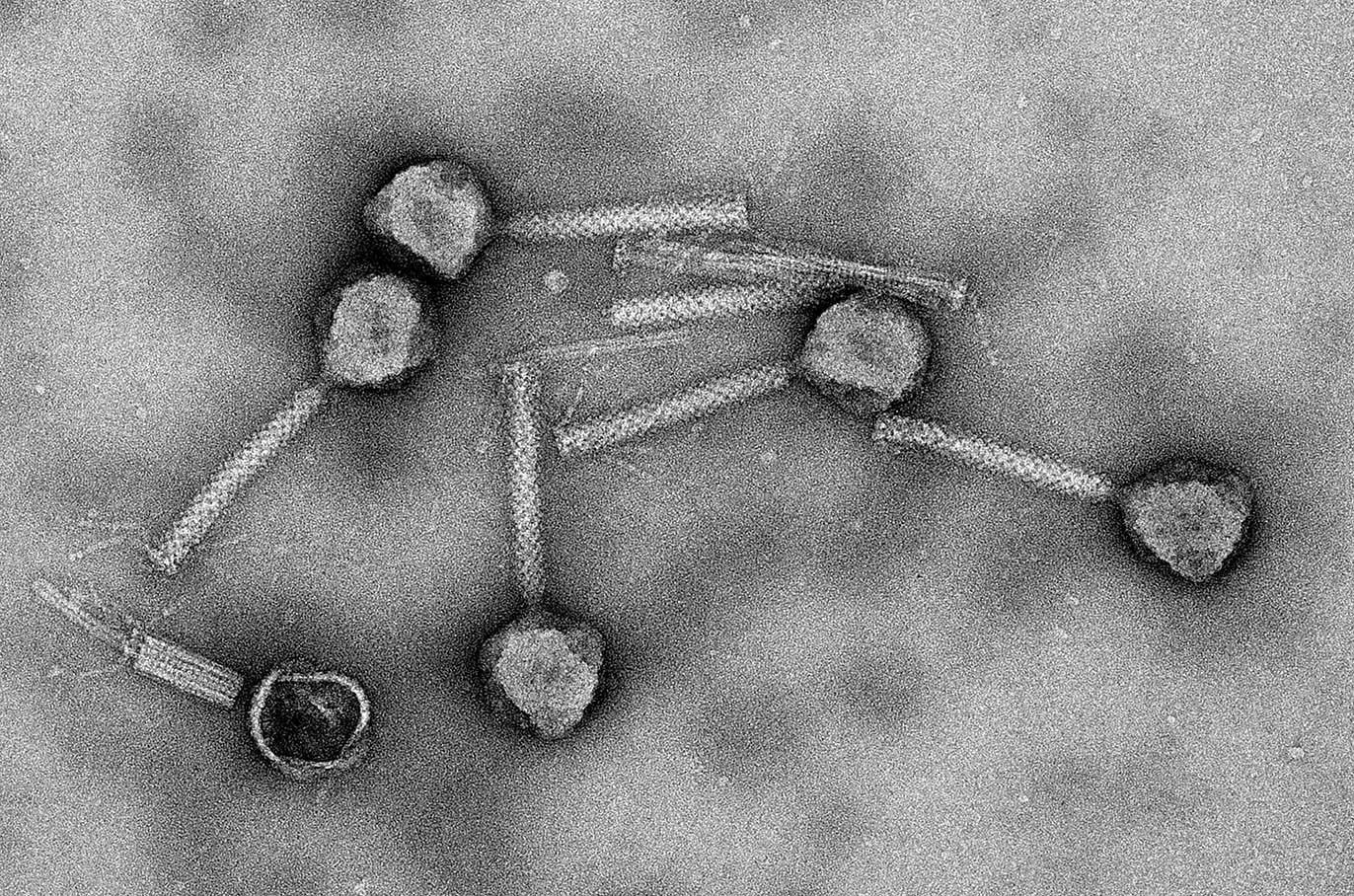
Verdedigingsmechanisme
Brouns, die sinds vier jaar in Delft werkt, richt zich met name op de interactie tussen bacteriën en bacterifagen. Daarvoor bestudeert hij de verschillende verdedigingsmechanismen die bacteriën gebruiken, waaronder CRISPR – clustered regularly interspaced short palindromic repeats. Dit is een afweermechanisme waarbij bacteriën een deel van het DNA van virussen die hen bedreigen in hun eigen DNA opnemen. Bij een volgende aanval herkennen ze het virus en kunnen ze sneller in actie komen. In feite treedt er dan resistentie op.
Fagen zijn echter ‘levende’ organismen en hebben een heel scala aan mogelijkheden om deze verdediging van bacteriën – ofwel deze resistentie – weer te omzeilen. Zo zijn bacteriën en bacteriofagen al miljoenen jaren in een wapenwedloop verwikkeld.

Fagencollectie
Daarnaast bouwt Brouns aan een non-profit fagenbank, een soort bibliotheek met fagen voor faagtherapie. Daarvoor isoleert en kweekt hij zelf bacteriofagen. Hij werkt samen met het Universitair Medisch Centrum Utrecht. Artsen sturen hem bacteriën van genezen patiënten en hij zoekt daar de faag bij die de bacterie kan bestrijden. Fagen zijn overal te vinden waar bacteriën zijn. De kunst is precies die faag te vinden die die ene bacterie kan bestrijden.
In zijn Fagenbank heeft Brouns ondertussen 120 fagen verzameld die geschikt zijn voor de bestrijding van negen bacteriën. Dat 120 fagen ‘maar’ negen bacteriën kunnen bestrijden in plaats van 120, kan Brouns gemakkelijk verklaren. ‘De bacterie kan zich verhullen in verschillende “jasjes” en om door deze jasjes heen te komen heb je steeds een andere bacteriofaag nodig. Het aantal jassen verschilt per bacterie, sommigen hebben wel negentig verschillende jassen, anderen maar drie of vier.’
MEER LEZEN OVER HOE BACTERIOFAGEN ONS KUNNEN HELPEN EN WAAROM DAT NOG NIET KAN?
Het volledige verhaal over bacterievirussen als levensredders en de tweede generatie faagtherapie vind je in het augustusnummer van De Ingenieur. Koop de digitale versie voor € 7,50, of neem - met een flinke korting van 25 % - een digitaal jaarabonnement van twaalf nummers voor € 69,-.
Tekst: Angèle Steentjes
Openingsfoto: Een bacteriofaag valt een bacterie aan. Foto: Depositphotos







