
Van CO2 naar nuttige stoffen met nanotechnologie
CO2 uit de lucht is om te zetten in verschillende nuttige stoffen, voor de opslag van energie en voor de chemische industrie. De Delftse promovendus Ming Ma onderzocht de processen voor het maken van deze stoffen. Nanodraadjes van verschillende metalen blijken verschillende eindproducten op te leveren.
Op zich is de CO2 die in de lucht zit een volkomen normaal verschijnsel. Het gas komt vrij bij de verbranding van natuurlijke materialen en dieren en mensen ademen het uit. Aan de andere kant nemen planten het juist weer op; een cyclus die al miljarden jaren oud is.
Alleen heeft de mens deze cyclus danig verstoord, met onze zware industrie, het vervoer en ons eetgedrag, waarvoor enorme hoeveelheden fossiele brandstoffen moeten worden verstookt. Dat heeft ervoor gezorgd dat de concentratie van het broeikasgas CO2 in de atmosfeer danig is opgelopen, met een snellere opwarming van de aarde tot gevolg. Het is duidelijk dat we daar iets aan moeten doen.
Opslaan in de bodem
Nu kun je CO2 uit rookgassen halen en in de bodem opslaan; dat helpt en onder meer Noorwegen doet dat al. Maar je zou ook iets nuttigs kunnen doen met de CO2, zie ook het grote verhaal ‘Koolstof wordt grondstof’ dat we hierover hadden in De Ingenieur van mei 2017.
Chemische producten
Promovendus Ming Ma koos zijn eigen aanpak; hij deed aan de TU Delft onderzoek naar de zogeheten elektroreductie van CO2, waarbij CO2 samen met water wordt omgezet in waardevolle chemische producten. Zie ook onderstaande illustratie (bron Ming Ma).
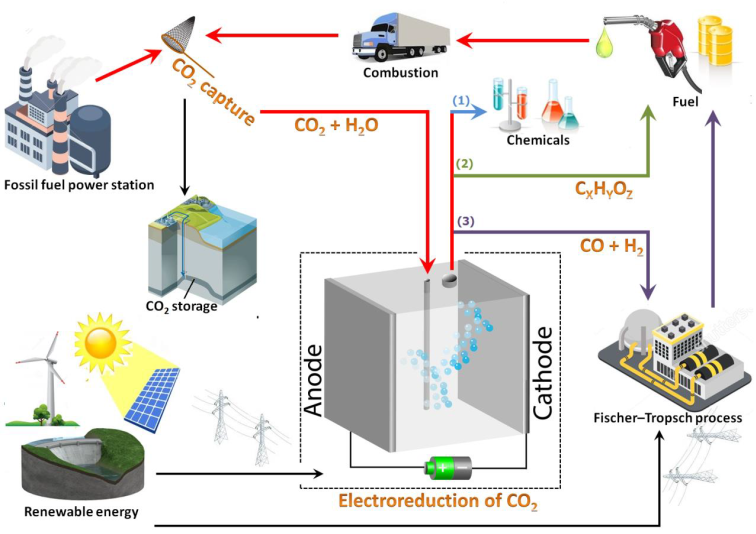
Ma onderzocht welke processen plaatsvinden op nanoschaal wanneer je verschillende metalen gebruikt bij de elektroreductie van CO2 (zie figuur hieronder). Daarvoor bouwde hij roosters van nanodraadjes van verschillende metalen, die fungeren als katalysator van de reactie. Maak je bijvoorbeeld nanodraadjes van koper, dan ontstaan er vooral koolwaterstoffen, terwijl de reactie bij het gebruik van nanoporeus zilver hoofdzakelijk CO oplevert.

Reacties reguleren
Wat Ma verder ontdekte, is dat de reacties vrij precies te reguleren zijn door te spelen met enkele parameters, zoals de lengte van de gebruikte nanodraden, hoe dicht ze op elkaar staan en de stroomsterkte door de draadjes. Zo kun je in theorie mengsels maken van koolwaterstoffen in de gewenste verhouding.
Als je voor de katalysator metaallegeringen gebruikt, komen er nog interessantere resultaten uit het proces. Zo blijkt een legering van platina en goud relatief grote hoeveelheden mierenzuur op te leveren (HCOOH) Dit is een veelbelovende stof voor het opslaan van groene energie; uit mierenzuur kan weer stroom worden gemaakt met brandstofcellen. Eindhovense studenten demonstreerden dit al eens met een auto en een bus op mierenzuur (lees: ‘Mierenzuur is brandstof voor de transportsector’ en ‘Auto op mierenzuur’)
Betaalbaar
Om deze processen uiteindelijk op grotere schaal toe te kunnen passen, is het wel van belang dat het uit de lucht halen van CO2 betaalbaar is (lees: ‘CO2-winning uit de lucht voedt paprika’s’). Dat kost nu nog honderden dollars per ton. ‘Dat is veel duurder dan je CO2 betrekken van elektriciteitscentrales of de bereiding van staal, die prijs moet dus fors omlaag’, zegt Ma.
Verder zijn er nog tal van technologische uitdagingen, weet Ma. ‘Voordat je deze processen op commerciële schaal kunt toepassen, moet je aan een aantal eisen voldoen. Zo moet je een hoge selectiviteit hebben voor het gewenste eindproduct en hoop je voldoende te hebben aan een lage spanning voor de elektroreductie. En uiteraard moeten de materialen over langere tijd stabiel blijven.’
Ming Ma verdedigt donderdag 14 september zijn proefschrift. Hij is de eerste die promoveert in de nog jonge onderzoeksgroep van Wilson Smith. Het vervolgonderzoek zal zich focussen op het verfijnen van de processen en het opschalen ervan.
Openingsbeeld Schematische weergave van de chemische processen die plaatsvinden aan het katalysatoroppervlak. Bron: Proefschrift Ming Ma







